têm-se lido e ouvido as mais diversas opiniões e leituras. Confesso que fico um pouco espantado, e se também tenho as minhas dúvidas nalguns aspectos (talvez por leitura superficial do relatório do OE), noutras há mesmo leituras apressadas dos números. Destaco duas leituras que me parecem enganadoras:
– decréscimo do orçamento da saúde em 17% – conclusão obtida directamente do quadro do OE 2013 que compara a dotação orçamental de 2012 (depois de orçamentos rectificativos) e de 2013. Esta comparação é errada se quisermos saber alguma coisa quanto ao que vai estar disponível para as instituições do Serviço Nacional de Saúde. O valor de 2012 neste quadro inclui verbas excepcionais para pagar as dívidas passadas acumuladas (infelizmente um aspecto não tão excepcional assim), logo essas verbas em 2012 não corresponderam a mais fundos para o funcionamento normal das instituições do SNS. Para saber do aperto financeiro (ou não) sobre o SNS em 2013 versus 2012 é necessário retirar esse valor. Grosso modo, serão perto de 2000 milhões de euros. E lá se vai a diferença de 17%. Mas um ponto melhor de comparação é provavelmente o que estava previsto no OE 2012 para o SNS em 2012, na medida em que corresponde ao que se pretendia transferir. Esse valor é inferior à transferência para o SNS no OE 2013. Só que também esta comparação não é inteiramente exacta – em 2012 não foi pago um subsídio aos funcionários públicos, incluindo os da saúde, que será pago em 2013 (por conta da decisão do Tribunal Constitucional). Logo o aumento da transferência do OE 2013 face ao OE 2012 para o SNS, expurgada das verbas das dívidas, ainda não é completamente correcto. Se admitirmos que grosso modo o valor deste subsídio a pagar aos funcionários públicos em 2013 que não foi pago em 2012 corresponde no caso da saúde a algo entre 300 e 400 milhões de euros (estimativa minha, uma vez que não encontrei uma estimativa oficial para este valor), então a transferência do SNS em 2013 é sensivelmente igual à de 2012. Há algumas imprecisões nestas contas, mas em termos gerais não se poderá falar de um aperto muito maior do que já existiu em 2012 ou numa folga e capacidade de desenvolvimento em 2013 face a 2012. Insistir nos 17% de redução é por isso pouco útil, e irrelevante para perceber o que se vai passar no SNS.
– poupanças com medicamentos – neste campo, aparece uma poupança prevista com a política do medicamento no “Quadro II.3.1. Medidas de consolidação orçamental em 2013”, p. 47 do Relatório do OE 2013, em 146 milhões de euros.
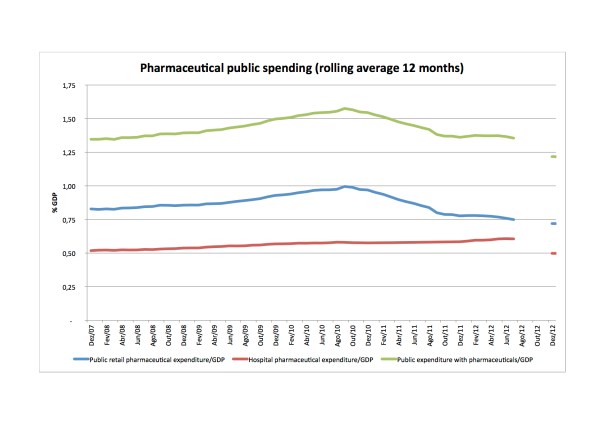
Ora, este valor de 146 milhões de euros não é compatível, só ele, com o objectivo de redução da despesa pública com medicamentos assumido como compromisso no Memorando de Entendimento – de acordo com o que consultei, o objectivo de despesa pública em ambulatório com medicamentos para 2012 é de quase 1200 milhões de euros (ver aqui, p. 4, cláusula 4.ª). O objectivo para 2013 em termos de despesa pública com medicamentos é de 1% do PIB, o PIB de referência para este efeito é 175 000 milhões de euros (cláusula 3.ª do acordo). Logo a despesa em 2013 deveria ser 1750 milhões de euros, face ao objectivo de 2012 de 2038 milhões de euros. A diferença entre os dois valores é 288 milhões de euros, muito acima dos 146 milhões previstos para a contribuição da política do medicamento. Uma interpretação possível é que estes 146 milhões dizem respeito à despesa em ambulatório, e o restante dos 288 milhões de euros (142 milhões) terá de vir do medicamento em ambiente hospitalar. Se esta interpretação não for válida, então deverá inferir-se que se abandonou o objectivo de 1% do PIB em termos de despesa pública com medicamentos. Não consegui encontrar informação no OE 2013 que me permitisse clarificar esta dúvida.
O que é dito sobre política do medicamento no OE 2013:
Política do Medicamento
- Promoção da prescrição, dispensa e utilização de medicamentos genéricos, nomeadamente através da conclusão do processo de implementação e dinamização da prescrição por Denominação
- Comum Internacional (DCI) e do reforço da monitorização da prescrição e da dispensa de medicamentos;
- Promoção do acesso ao mercado de medicamentos genéricos;
- Reforço da monitorização da utilização dos medicamentos, potenciada pela publicação das normas e orientações clínicas relativas ao medicamento;
- Continuação da publicação e promoção de normas de orientação clínica, tanto no que se refere ao medicamento como relativamente a MCDT, e respetivo sistema de auditoria da sua implementação;
- Consolidação, disseminação e monitorização da prescrição eletrónica, com implementação do processo de desmaterialização da prescrição e da faturação de medicamentos e MCDT;
- Promoção de eficiência e aumento da capacidade negocial na aquisição de medicamentos, dispositivos médicos e outros bens e serviços, através de aquisições partilhadas e/ou centralizadas;
- Monitorização centralizada do consumo intra-hospitalar de medicamentos e MCDT, com vista à otimização de recursos e análise custo-benefício;
- Monitorização do acordo com a indústria farmacêutica em relação à limitação de encargos públicos com medicamentos em ambulatório e meio hospitalar;
- Realização da revisão anual de preços com base em preços internacionais, e monitorização da remuneração de distribuidores farmacêuticos e de farmácias;
- Implementação de novas formas de monitorização e de prevenção da fraude.