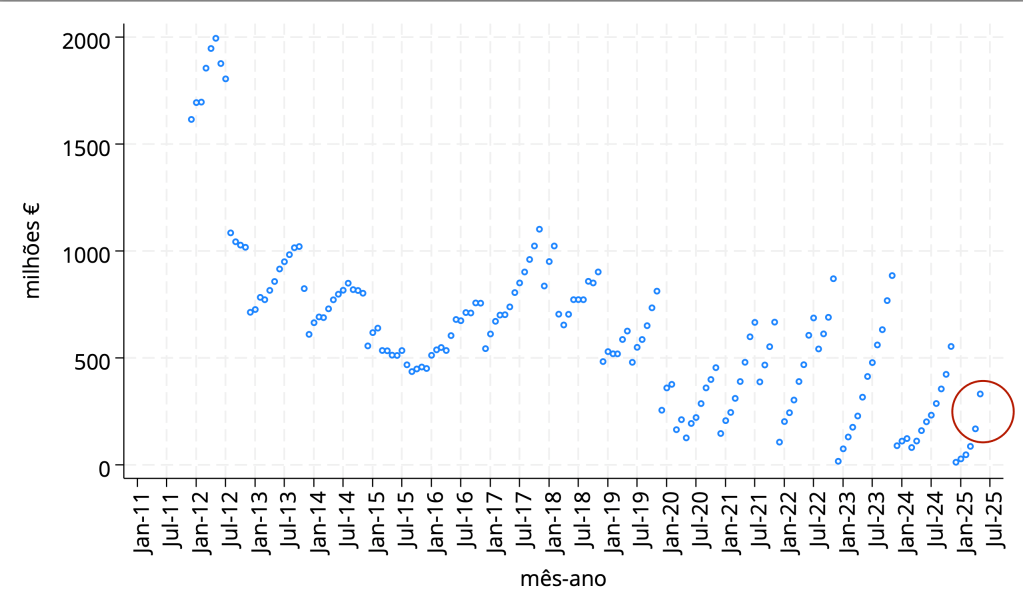
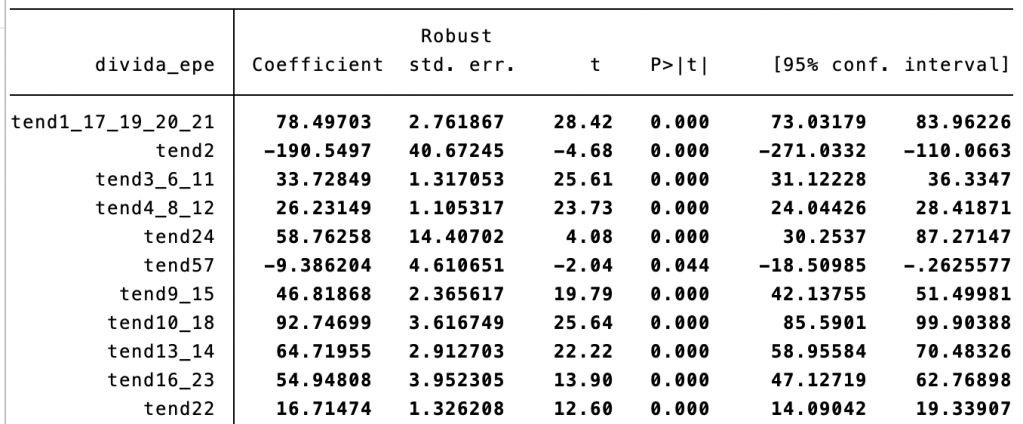
A Exigo promoveu e organizou há cerca de um mês uma conferência sobre os 10 anos do SiNATS – Sistema Nacional de Avaliação de Tecnologias de Saúde – com base em análise própria, colocada à discussão geral.
A Exigo fez um esforço meritório de perceber os efeitos do SiNATS, usando dados públicos apenas, permitindo total replicabilidade da análise (o que é um elemento importante da credibilidade do trabalho realizado).
Há um dificuldade metodológica base (usual): conseguir definir o que teria sucedido na ausência do SiNATS. A comparação antes/depois pode não ser suficiente, sobretudo na presença de tendências, que podem mudar ou não, e em que mesmo não se alterando levam a médias diferentes antes e depois da introdução do SiNATS.
O estudo considera 7 áreas de análise (corresponde aos 7 objetivos do SiNATS): ganhos em saúde, uso eficiente de recursos públicos, sustentabilidade financeira do SNS, reduzir desperdício, promover inovação relevante, promover equidade e monitorizar efetividade das tecnologias
As várias áreas cruzam-se, olhemos para o que a Exigo consegue tratar.
Sobre cada área:
Ganhos em saúde
Utilizam-se indicadores agregados: Esperança de vida – seria importante ter os anos antes do SiNATS, admitir a possibilidade de ter rendimentos marginais decrescentes, ter a possibilidade de a tendência se ter alterado, ou ser um salto num momento, ou até ter comparação com um país sem SiNATS. Estes elementos permitiriam dar mais conteúdo à análise.
É dificil argumentar que possa ter um efeito visível na série estatística, apesar da visão positiva que possa existir.
Como os efeitos sobre a mortalidade podem demorar a produzir-se, havendo também muitos outros canais de influência sobre a mortalidade, caso houvesse informação, a utilização de anos de vida ajustados pela incapacidade, para doentes de cada patologia associada com medicamentos introduzidos (ou em que tenha sido recusada a introdução) no âmbito do SNS, face ao que seria a decisão no sistema de aprovação que existiria na ausência do SiNATS, estaria mais perto de uma avaliação mais precisa. Contudo, há aqui demasiados “se” para que seja possível concretizar hoje em dia esta avaliação.
Sustentabilidade financeira do SNS
Seria adequado uma abordagem similar à descrita no ponto anterior, em procurar olhar para evolução de série estatística. Mas aqui o contexto antes/depois da criação do SiNATS é bastante diferente.
É expressa uma visão positiva baseada em estabilidade do rácio despesa em medicamentos face ao total da despesa pública.
Na lógica de perceber o contrafactual da decisão de criar o SiNATS, teria sido possível “estimar” para alguns casos a decisão de preços que teria ocorrido para o caso de novos medicamentos (inovadores ou não), na ausência do SiNATS?
No caso da despesa pública em saúde, quer no período pré- quer no período com SiNATS há demasiados eventos simultâneos, desde logo o período de resgate internacional de Portugal antes do SiNATS e a pandemia depois do SiNATS. Torna complicado extrair muita informação sobre o SiNATS a partir de séries agregadas de despesa em saúde.
Em qualquer caso, é dificil antecipar que o efeito da criação do SiNATS pudesse ser negativo, não sendo evidente qual o mecanismo pelo qual isso pudesse ter lugar.
Utilização de recursos públicos
Este objetivo poderia ser facilmente junto com a noção de desperdício.
O documento Exigo toma uma visão baseada no tempo médio de aprovação de decisões. Aqui teria sido útil condicionar de alguma forma no número de pedidos de decisão remetidos à CATS (tempo médio dependente do número de pedidos entrados).
Seria igualmente útil ter um elemento de qualidade da decisão, que só pudesse ser realizada com intensa utilização de recursos (tempo e pessoas), ainda que pudesse ser por amostragem (e não todas as decisões).
De um ponto de vista geral, com efeitos de aprendizagem, os processos associados ao SiNATS deveriam ter melhorado ao longo do tempo, com rotação dos peritos usados.
A eficiência do SiNATS é vista como sendo o resultado de uma “produção” face aos recursos usados para a produzir. Numa visão mais detalhada, é importante considerar efeitos de economias de escala e de economias de aprendizagem, bem como a qualidade das decisões.
Efetividade das tecnologias
Há uma abordagem baseada numa revisão sistemática da literatura.
Não há um esforço sistemático de sector público em perceber a efetividade das tecnologias aprovadas, como resultado dessa revisão sistemática da literatura. Esta conclusão é baseada no baixo volume de documentos que o processo de revisão sistemática da literatura produziu para análise. É um tema “desaparecido em combate”.
De um ponto de vista pessoal, conjecturo que não fosse diferente se não houvesse SiNATS. Dada a falta de recursos humanos para realizar esta monitorização, provavelmente não seriam redirecionados esforços para esta monitorização de outras áreas de atuação caso não estivesse em vigor o SiNATS (só sucederia caso o SiNATS absorva muito mais recursos do que um sistema alternativo que pudesse ser usado, o que podendo suceder não surge como plausível).
Reduzir o desperdício
Há decisões negativas justificadas e foram retirados do mercado produtos de baixo valor.
Ainda assim, há referência a um aumento do desperdício, com aprovação a preços elevados de medicamentos de baixo ou nenhum valor terapêutico acrescentado. O mesmo pode ser dito para dispositivos médicos.
A opção de análise da Exigo incidiu sobre a velocidade das decisões de financiamento público.
A conclusão é a de se observar uma maior velocidade antes do SiNATS. Mas a pergunta (a fazer neste contexto) é se na ausência do SiNATS teria sido diferente. Idealmente devia-se ter também em conta os recursos disponíveis para apoiar a decisão.
Do ponto de vista de pressão para a negociação, as pressões orçamentais não teriam sido diferentes se o SiNATS não tivesse sido criado.
A avaliação feita deve ser complementada com elementos adicionais, ou pelo menos referidos esses elementos, caso não estejam publicamente disponíveis.
Promover inovação relevante
Portugal é irrelevante para as linhas de inovação internacional.
Este objetivo é visto como acesso a inovação por parte dos doentes. Há um tempo mais rápido de decisão em caso de medicamentos inovadores, mas não é suficiente distinto (em termos estatísticos, indicando que a variabilidade é considerável).
Mas também se poderia olhar para ver se o preço é maior para medicamentos mais inovadores.
Continua a fazer falta a perspectiva de contrafactual adequado, face ao papel da EMA, que também se pode ter modificado ao longo do período.
A conclusão é que não houve grande diferença em termos de maior rapidez de aprovação de medicamentos inovadores depois da criação do SiNATS. Não é um resultado que surpreenda, e daí a importância de olhar para os preços.
Acesso equitativo
A equidade é vista entre grupos de medicamentos e dentro de cada grupo de medicamentos. É uma boa forma de identificar potenciais diferentes efeitos.
É usado um único indicador associado ao tempo de decisão.
Partilha os aspectos metodológicos já referidos anteriormente.
Seria interessante saber se houve grupos de doentes que ficaram de fora, falta de acesso, em consequência das decisões tomadas. Se tal não foi o caso, o tempo de acesso fica como a dimensão mais relevante a ser desenvolvida na análise.
Há uma conclusão global ambígua, amplificada pela ausência de uma análise contrafactual (que tipo de resultados teria gerado o processo usado em alternativa ao SiNATS?)
Das intervenções do painel, alguns aspectos que retive, sem ordem específica:
1 Destacada a importância da consistência dos dados para conhecer o real estado de saúde da população, antes e depois do SiNATS.
2 A possibilidade de usar comparação internacional para perceber as desigualdades de acesso a novos medicamentos entre países.
3 Tendo-se focado várias vezes no tempo de aprovação, há um elemento que seria bom conhecer – qual o tempo óptimo de decisão, dado que se tem de encontrar um equilíbrio entre uma decisão fundamentada e sem erros (requere mais tempo) e uma decisão que dê acesso mais rápido (requere menos tempo)? O “erro” de falhar no tempo de acesso não tempo o mesmo peso do “erro” de aprovar uma tecnologia que não o deveria ser. Não era algo a que estudo devesse responder. É uma ideia para discussão futura, de forma a enquadrar a avaliação dos tempos de decisão.
4 Parte do tempo de atraso no acesso em Portugal depende da decisão das companhias na submissão dos pedidos (que variam entre 1 semana e quase 2 anos, desde que o produto é aprovado pela EMA, segundo comentário feito no período de debate).
5 Como é usual, é referida a necessidade de recursos (mais contratações e disponibilidade de peritos), bem como problemas na informação submetida pelas empresas, havendo espaço para haver mais clareza quanto ao volume de informação adequado a fornecer para uma avaliação de novos medicamentos (e o tratamento dessa informação afeta naturalmente os tempos de decisão). Sendo “fácil” apelar a ter mais recursos, é preciso evitar que esse argumento substitua completamente a possibilidade de revisitar processos para os melhorar. Em geral, e não apenas neste contexto, ao longo do tempo vão-se adicionando “frições” (regras adicionais), muitas vezes justificadas pontualmente por problemas que foi preciso resolver, mas que com o pena se tornam penalizadoras e desnecessárias.
6 Sobre mecanismos de pagamento / reembolso dos novos medicamentos, há ainda muito espaço para melhoria. Sobretudo têm de ser pensados com cuidado, em termos do problema que procuram resolver e das infraestruturas de informação que são necessárias para os resolver. Por exemplo, em acordos de partilha de risco, com preço condicional a desempenho, está-se a querer resolver problemas de informação sobre a qualidade do produto? Com ou sem informação assimétrica (a empresa conhecer mais ou o mesmo que o pagador)? Ou é incerteza sobre o volume de procura, e o que se pretende é “segurança orçamental” do pagador? São dois problemas económicos distintos que podem pedir resposta diferentes.
7 Sobre eventual revisão do SiNATS, assusta-me sempre ter alterações casuísticas e pouco pensadas, apenas para dar resposta a pressão pública. O tempo de reflexão necessário para que haja pensamento e discussão não é compatível com o tempo mediático. Mas é necessário que exista esse tempo de pensamento para evitar alterações que tenham resultados inesperados e para que todos os efeitos possam ser antecipados e ponderados. Mesmo atendendo a que a discussão alargada que houve quando se criou o SiNATS gerou expectativas que depois a legislação produzida não refletiu, convém ver com atenção que novas expectativas e possibilidades se criam com uma revisão do SiNATS. Rever com calma (e rapidez compatível com ponderação) deverá ser o caminho dessa eventual revisão.
8 Sobre estruturas de dados, há que ultrapassar o ter estruturas de dados do século XX se queremos aproveitar plenamente as vantagens do espaço europeu de dados em saúde (e para isso é igualmente preciso ultrapassar a mentalidade medieval do “meu castelo de dados”).
9 É relevante estabelecer e agilizar mecanismos de avaliação de novos medicamentos em vida real. Os resultados podem ser substancialmente distintos do que sucede em ensaios clinicos (e não por causa da falta de qualidade dos ensaios clinicos, há muitos elementos que não devem estar nos ensaios clinicos para estes produzirem a informação que é necessária, e que depois influenciam a forma como se produzem efeitos na utilização real, basta pensar nas muitas combinações de doenças crónicas que as pessoas possam ter e/ou nos comportamentos individuais e a forma como eventualmente interferem na eficácia dos medicamentos). Essa informação de “vida real” será cada vez maior, e é preciso construir a forma de a utilizar de modo útil fazendo e melhorando. Há uma aprendizagem que só se consegue pela prática.